アスベストにくっついて光らせる画期的な検出法やツールを独自開発。
黒田先生の研究室では、「界面とバイオ」「リンとバイオ」「シリコンとバイオ」の3つの領域について研究を進めている。いずれも環境バイオテクノロジーや健康に資するバイオセンシング※の開発を目指すものだ。ここでは、「界面とバイオ」の領域での研究について紹介しよう。
※生体や生体分子の持つ優れた分子認識能力を活用した計測技術のこと

黒田先生の名を一躍有名にした研究といえば、「アスベスト」を光らせて検出する「バイオ蛍光法」の開発である。開発のきっかけは、2005年くらいから注目されるようになった「アスベスト問題」だ。アスベストは繊維状の鉱物で、建材として古くから重宝されてきたが、生産や建築作業に携わった人たちの健康被害が明るみになり、人体に有害であることが知られるようになった。現在では先進国の大半で全面使用禁止となっているものの、古い建物にはアスベストを含む建材がいまだに残されており、解体の際に飛散する危険性があるため、現場でアスベストをモニターする必要がある。アスベスト問題はいまも続く喫緊の問題なのだ。
これに対して、従来のアスベストの検査は熟練を要し、最終的には電子顕微鏡とX線による元素分析で同定するという複雑なもので、より迅速な検出方法が求められていた。そこで、先生の研究グループではアスベストを見分けるタンパク質/ペプチドが開発できれば、検査が迅速におこなえると考え、アスベストに結合するタンパク質を発見するに至る。 「アスベストをモニターする抗体ができればいいのですが、無機の固体なので難しい。抗体に代わるものとして、アスベストと特異的に結合するタンパク質を探しました。それまでの研究で、シリコン半導体と結合するタンパク質を見つけていたので、シリコンの一種であるアスベストにも見つかるのではと考えたのです」
さらにこのタンパク質を可視化するために、このアスベスト結合タンパク質と蛍光タンパク質とを遺伝子操作によって結合させ、アスベストを光らせることに挑み、生まれたのが『バイオ蛍光法』である。
 バイオで光るアスベスト
バイオで光るアスベスト
 持ち運べるiPad蛍光顕微鏡
持ち運べるiPad蛍光顕微鏡
2010年にはこうした研究の成果を「アスベスト検出キット」としてリリース。2016年には、現場に熟練者がいなくてもiPadの通信機能を使って検査室からリアルタイムで判定のサポートができる、画期的な可搬型蛍光顕微鏡の開発にも成功する。そして、『バイオ蛍光法』は2017年に環境省指定の「公定法」に認定される。これらの研究は、“バイオテクノロジーと無機物とをつなぐ”、まさに世界初の研究であった。
 2012年/文部科学大臣表彰(左)と
2012年/文部科学大臣表彰(左)と2017年/産官学連携功労者表彰記念 環境大臣賞
エクソソームの回収・精製の手法を開発。分析や医療応用に役立てる。
さらに先生の研究室では、石田講師と共に「エクソソーム」の研究にも取り組んでいる。エクソソームとは、細胞から分泌される直径30~120nm程度の脂質二重層膜に覆われた細胞外小胞だ。内部には細胞の情報が高度に保存されており、血液中からこれを集めて調べれば、細胞がどのような状態であるかがすぐに分かるという。「エクソソームは膜に覆われているため分解されにくく、情報が保存されたまま出てくるので、これを調べて、ガンなどの新たなバイオマーカーにしたり、エクソソームそのものを治療薬として利用するといったような研究が世界中で活発に行われています」と先生。課題となるのは、エクソソームの回収法(精製法)だ。疾患の治療に利用するには、損傷の少ないエクソソームを精製する必要があるほか、実用規模で効率良く精製するシステムの開発が必要であった。
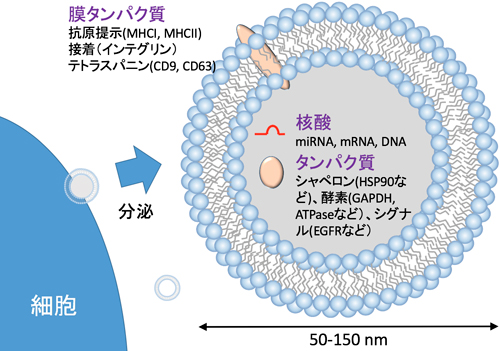 エクソソーム概念図
エクソソーム概念図
そこで先生たちが考えたのは、脂質二重層膜という有機の界面に結合するペプチドを利用する方法だ。
「エクソソームの膜に親和性のあるペプチドとして、最終的に8残基のリジンを含むペプチド(リジンペプチド)が最適であることが分かりました」
EXペプチドと名付けられたこのペプチドを磁性ビーズに固定化することで、血清や培養液から、損傷の極めて少ないエクソソームを回収・精製することができるという。先生たちはこのペプチドを使った「エクソソーム精製キット」や「エクソソーム自動精製システム」を作製し、すでに市販されている。また、「大量精製用カラム」も作製し、エクソソームの分析にも貢献しようとしている。
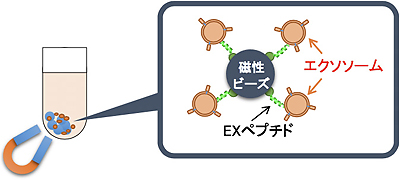 EXペプチドを用いたエクソソームの精製概念図
EXペプチドを用いたエクソソームの精製概念図
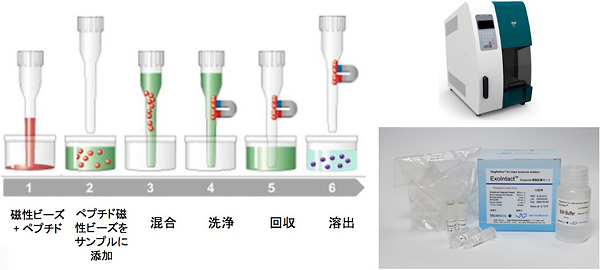 エクソソーム自動精製システム
エクソソーム自動精製システム
共通するのは「平面を捉える」ということ。自然界には存在しない新しいものに挑む。
この研究の特徴は、「平面を捉えるペプチド」を活用するところにある。ところがそれは、自然界には存在しないものだという。アスベストにくっつくタンパク質/ペプチドも、自然界には原理的にはないものだ。
「生物の中ではタンパク質とタンパク質の認識、結合というのはいっぱいありますが、いずれも構造が複雑で、その凸凹を認識するように進化してきているんですよね。だから、平面というのは細胞の中にはないんです。細胞の中にアスベストがないのと同じで、あっても意味がない」と先生。

一方で、「ペプチドにはものすごい可能性がある」とその魅力を説く。
「もしペプチドが100個続いたら何種類あるかというと、20種類あるアミノ酸が100個なので20の100乗です。それは、10の90乗ほどと言われている宇宙の原子の数よりもはるかに多いんですよ。宇宙が全部ペプチドになったとしても種類をカバーできない。それほどペプチドの種類というのは恐ろしく多くて、人間はほぼ100%知らないと言えます。誰も知らないけれども、ランダムに組み合わせるといろいろなものができる。自然界にないものができるんですよ」
先生によれば、『平面を認識するペプチドの研究』というのは世界を見てもあまり例がない希少な研究とのこと。
「平面のひとつにアスベストがあるし、エクソソームというのも、脂質二重膜という平面、その他、いろんな無機物や半導体などの『平面』を捉えるペプチドを我々は探しています。未知のものがたくさんあるペプチドの中から、平面に結合するようなペプチド、世の中になかったようなペプチドを取ってきて、役に立つものを作り出して応用していくというのがこの研究のコンセプトです」
「世の中になかったものを作り出すことがおもしろく、それが世の中の役に立てば大変うれしい」と語る黒田先生。一番の喜びは、「どうやってそんなことを考えたのか?」と尋ねられることだと言い、「今後も、世の中に役立つものを作り続けたい」と微笑む。最後に、「大学は多様性が大事。若い人たちには目先の実績よりも『誰もやらない研究』を勇気を持って始めてほしい」と語った。
■YouTube
 2021年7月12日掲載
2021年7月12日掲載


